Опанувавши матеріал параграфа, ви зможете:
• називати ознаки класифікації хімічних реакцій; типи хімічних реакцій, класифікованих за зміною кількості та складу реагентів і продуктів реакцій;
• розрізняти ознаки класифікації; реакції сполучення, розкладу, заміщення й обміну;
• характеризувати хімічні реакції різних типів;
• наводити приклади хімічних реакцій різних типів;
• складати рівняння реакцій різних типів.
Ознаки класифікації хімічних реакцій. У 7-8 класах ви ознайомилися з великою кількістю хімічних реакцій, що відбуваються за звичайних або відповідних для їхнього перебігу умов. Вивчення теми «Хімічні реакції» допоможе вам упорядкувати свої знання про реакції на основі ознак, за якими вони об’єднані в групи (рис. 44).
Пригадайте, які типи хімічних реакцій уже вам відомі.

Типи хімічних реакцій за ознакою кількості та складу реагентів і продуктів реакції. Залежно від того, які речовини вступають у реакцію та які утворюються під час її перебігу, хімічні реакції поділяють на реакції сполучення, розкладу, заміщення й обміну.
Реакції сполучення. У реакції сполучення вступають прості та складні речовини з утворенням однієї складної речовини. Вам уже відомо, що метали проявляють здатність реагувати з неметалами. Результатом таких реакцій є утворення оксидів або солей. Повторимо реакції сполучення за допомогою демонстраційних дослідів.

Дослід 1. Взаємодія заліза із сіркою. Змішаємо у фарфоровій чашці порошок заліза й порошок сірки в масовому співвідношенні 7 : 4. Нагріємо їх у полум’ї спиртівки до початку реакції. Далі вона відбувається самовільно з виділенням тепла. Після охолодження утворюється нова речовина ферум(ІІ) сульфід (рис. 45).
Рівняння реакції: Fe + S = FeS.
Дослід 2. Взаємодія сірки з киснем. Нагріємо порошок сірки до температури займання й розмістимо його в заздалегідь підготовленій колбі з киснем. Сірка згоряє яскравим полум’ям (рис. 46).

Дослід 3. Взаємодія кальцій оксиду з водою. Покладемо у фарфорову чашку кальцій оксид і доллємо воду. Відбувається реакція з утворенням кальцій гідроксиду: CaO + H2O = Ca(OH)2 Усі три реакції належать до реакцій сполучення. Загальне рівняння реакції: А + В = С.
Вам уже відомо, що в реакції сполучення вступають складні речовини. Зокрема, деякі оксиди металічних і неметалічних елементів реагують з водою. Наприклад, під час реакції BaO + H2O = Ba(OH)2 утворюється барій гідроксид. За наявності кисню нітроген(^) оксид з водою утворює нітратну кислоту:
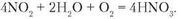
Сформулюйте самостійно визначення реакцій сполучення на основі рівнянь реакцій взаємодії заліза із сіркою та горіння сірки в кисні.
Реакції розкладу. Із цим типом хімічних реакцій ви ознайомилися під час вивчення теми «Добування кисню в лабораторії»
(7 клас), розкладаючи гідроген пероксид та інші речовини. Вам відомо, що за нагрівання основи й амфотерні гідроксиди розкладаються з утворенням відповідного оксиду та води. На оксид і воду розкладаються нестійкі кислоти.

Напишіть самостійно рівняння згаданих вище реакцій.
Яскравим прикладом є реакція розкладу амоній дихромату (NH4)2Cr2O7 (рис. 47), відома в хімії під назвою «хімічний вулкан» (рис. 48). Проведемо демонстраційний дослід.
Дослід 4. Розклад амоній дихромату. На керамічну підставку (плитку) насиплемо подрібнені кристали амоній дихромату, який має характерне яскраво-оранжеве забарвлення, надаючи їм форми гірки (див. рис. 47).
Посередині гірки вставимо 4-5 головок сірників і запалимо їх (замість сірників можна взяти розжарену скляну паличку). Починається реакція, яка супроводжується бурхливим розкладом солі. Гірка помітно збільшується внаслідок виділення азоту й водяної пари й утворюється пухка маса хром(ІІІ) оксиду темно-зеленого кольору. Рівняння реакції:
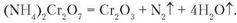
Загальні рівняння реакцій розкладу подаємо так:
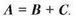
Сформулюйте самостійно визначення реакцій розкладу.
Реакції заміщення. Назва цього типу реакцій говорить про те, що під час їх перебігу відбувається заміщення одних атомів на інші в складній речовині. Такі реакції спостерігають при взаємодії металів з розчинами кислот, металів із солями.
Проведемо дослід, що демонструє перебіг реакцій заміщення.

Рис. 49. Реакції заміщення: а — між кислотою та цинком; б — між купрум(ІІ) сульфатом і залізом
Дослід 5. Взаємодія цинку з хлоридною кислотою. На дно хімічної склянки покладемо кілька гранул цинку та доллємо хлоридну кислоту (або розчин сульфатної). Через певний час цинк укривається пухирцями газу, який починає інтенсивно виділятися (рис. 49, а). Цинк заміщує атоми Гідрогену в кислоті. Відповідно утворюється сіль цинк хлорид і виділяється водень:

Опишіть самостійно реакцію, зображену на рисунку 49, б. Складіть рівняння реакції та сформулюйте визначення цього типу реакцій.
Загальне рівняння реакції заміщення: А + ВС = АС + В.
Реакції обміну. Вивчення теорії електролітичної дисоціації поглибило ваші знання про реакції обміну в розчинах електролітів. Під час їх перебігу здійснюється обмін складовими частинами речовин (див. § 12, 13).
Зрозуміло, що реакції цього типу відбуваються між двома складними речовинами. До них належать і відомі вам реакції на виявлення катіонів та аніонів у складі речовин. Проведемо для прикладу якісну реакцію виявлення сульфат-аніону.
Дослід 6. Взаємодія розчинів калій сульфату й барій гідроксиду. Наллємо в пробірку розчин калій або натрій сульфату об’ємом 2,5-3 мл, додамо розчин барій гідроксиду. Випадає білий, нерозчинний у кислотах осад барій сульфату (див. рис. 42, с. 84). Це ознака того, що реакція відбулася.
Напишіть самостійно рівняння реакції в молекулярній і йонній формах, сформулюйте визначення реакцій обміну.
Загальне рівняння реакції обміну: АВ + CD = AD + CB.
Отже, за ознакою зміни кількості та складу реагентів і продуктів реакції розрізняють чотири типи реакцій: сполучення, розкладу, заміщення й обміну.
ПІДСУМОВУЄМО ВИВЧЕНЕ
• Є кілька ознак класифікації хімічних реакцій: 1) зміна кількості та складу реагентів і продуктів реакції; 2) зміна ступенів окис-нення елементів, що входять до складу речовини; 3) тепловий ефект реакції; 4) напрям перебігу.
• За зміною кількості та складу реагентів і продуктів реакції розрізняють чотири типи хімічних реакцій: сполучення, розкладу, заміщення, обміну.
• Загальне рівняння реакції сполучення — А + В = С.
• Загальні рівняння реакцій розкладу можна подати так:
А = В + С.
• Загальне рівняння реакції заміщення — А + ВС = АС + В.
• Загальне рівняння реакції обміну — АВ + СD = АD + CB.
ЗАВДАННЯ ДЛЯ САМОКОНТРОЛЮ
1. Назвіть ознаки, за якими класифікують хімічні реакції.
2. Сформулюйте визначення реакцій: а) сполучення; б) розкладу; в) заміщення; г) обміну.
3. Допишіть праві частини молекулярних рівнянь, складіть йонно-моле-кулярні рівняння реакцій (де це можливо):
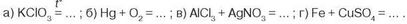
4. Допишіть праві частини молекулярних рівнянь, складіть йонно-молекулярні рівняння реакцій (де це можливо) і вкажіть, до якого типу вони належать:
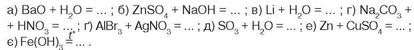
5. Напишіть рівняння реакцій між попарно взятими речовинами, де можливо, складіть йонно-молекулярні рівняння: а) барій нітрат і натрій сульфіт; б) алюміній і бром; в) кальцій хлорид і арґентум(І) нітрат; г) калій і вода.
6. Обчисліть об’єм водню (н. у.), що виділиться під час взаємодії натрію масою 11,5 г з водою.
7. Алюміній кількістю речовини 0,25 моль повністю прореагував із сіркою. Обчисліть масу й кількість речовини продукту реакції. Назвіть утворену речовину.
8. Напишіть рівняння реакцій за поданою схемою:

Обчисліть
масу утвореного барій гідроксиду, якщо в реакцію вступив барій масою 27,4 г
ЦІКАВО ЗНАТИ
На хімічному виробництві часто утворюються шкідливі речовини, які потрапляють у довкілля. Це зумовило появу нової науки — екологічної хімії (або «зеленої хімії»). Вона є філософією хімічних досліджень та інженерії, що закликає до створення продуктів і процесів, які допоможуть мінімізувати використання та виробництво шкідливих речовин. Мета екологічної хімії — зменшити забруднення та запобігти йому вже на стадії розробки хімічних технологій
Це матеріал з підручника Хімія 9 клас Савчин