Класифікація неорганічних сполук
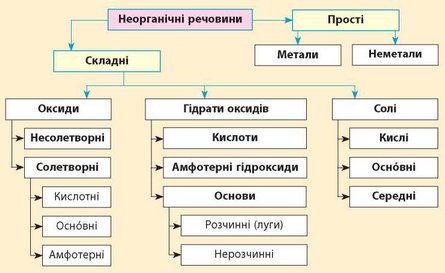
За певними спільними ознаками неорганічні речовини об’єднують в окремі класи (схема 1). Знаючи, до якого класу належить речовина, можна передбачити її властивості.
Схема 1. Основні класи неорганічних сполук
Оксиди
Оксиди — це бінарні сполуки з Оксигеном, у яких Оксиген виявляє ступінь _ окиснення -2.
Залежно від валентності хімічного елемента, що утворює оксид, склад оксидів може бути різним.
Загальна формула оксидів:
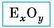
Розрізняють такі оксиди:
Солетворні:
• основні — оксиди, яким відповідають основи (утворені металічними елементами у ступені окиснення зазвичай +1 або +2: Na2O, FeO, CaO);
• кислотні — оксиди, яким відповідають кислоти (утворені не-металічними елементами: CO2, SO2, SO3, N2O5 та металічними елементами зі ступенем окиснення вище за +3: CrO3, Mn2O7, PbO2);
• амфотерні — оксиди, яким відповідають амфотерні гідроксиди (утворені деякими металічними елементами з проміжними між металічними та неметалічними властивостями: Al2O3, BeO, ZnO, Fe2O3,
Cr2O3);
Несолетворні: оксиди, яким не відповідають ані основи, ані кислоти (утворені деякими неметалічними елементами в проміжних ступенях окиснення: N2O, NO, CO, SiO).
Залежно від того, до якої групи належить оксид, він виявляє різні хімічні властивості (табл. 1).
Таблиця 1. Хімічні властивості оксидів*
|
Основні |
Амфотерні |
Кислотні |
|
Взаємодія з кислотами й основами |
||
|
Взаємодіють з кислотами з утворенням солі й води: CaO + 2HCl = = CaCl2 + H2O Не взаємодіють з основами |
Взаємодіють з кислотами й основами з утворенням солі й води: ZnO + 2HCl = ZnCl2 + H2O ZnO + 2NaOH = = Na2ZnO2 + H2O |
Взаємодіють з основами з утворенням солі й води: SO3 + Ca(OH)2 = = CaSO4 + H2O Не взаємодіють з кислотами |
|
Взаємодія з водою |
||
|
Оксиди лужних і лужноземельних елементів взаємодіють з водою з утворенням лугів: CaO + H2O = Ca(OH)2 Інші оксиди з водою не реагують: FeO + H2O * |
Не взаємодіють з водою |
Взаємодіють з водою з утворенням кислоти (за винятком силіцій(^) оксиду): SO3 + H2O = H2SO4 SiO2 + pO * |
|
Основні |
Амфотерні |
Кислотні |
|
Взаємодія з оксидами |
||
|
Взаємодіють з кислотними оксидами з утворенням солі: CaO + CO2 = CaCO3 Не взаємодіють з основними оксидами |
Взаємодіють з кислотними й основними оксидами та між собою: ZnO + SiO2 = ZnSiO3 ZnO + CaO = CaZnO2 ZnO + Al2O3 = Zn(AlO2)2 |
Взаємодіють з основними оксидами з утворенням солі: SO3 + CaO = CaSO4 Не взаємодіють з кислотними оксидами |
Кислоти
Кислоти — сполуки, що складаються з атомів Гідрогену, здатних заміщуватися атомами металічних елементів, та кислотних залишків.
Загальна формула кислот:
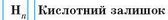
За різними ознаками кислоти класифікують на групи:
• за числом атомів Гідрогену в молекулах (основністю): одноосновні: HCl, HNO3;
двохосновні: H2S, H2SO4; трьохосновні: H3PO4;
• за вмістом атомів Оксигену в молекулах: оксигеновмісні: HNO3, H2SO4, H3PO4; безоксигенові: HCl, H2S, HF.
Оксигеновмісні кислоти є продуктами приєднання молекули води до молекул кислотних оксидів. Безоксигенові кислоти — це розчини деяких газів у воді. Хлоридна кислота — це розчин газуватого гідроген хлориду HCl у воді, флуоридна — розчин гідроген флуориду HF тощо.
Таблиця 2. Забарвлення деяких індикаторів у розчинах з різним середовищем
|
Індикатор |
Забарвлення в середовищі |
||
|
кислотному |
нейтральному |
лужному |
|
|
Лакмус |
Червоний |
Фіолетовий |
Синій |
|
Метиловий оранжевий |
Червоний |
Оранжевий |
Жовтий |
|
Фенолфталеїн |
Безбарвний |
Безбарвний |
Малиновий |
Основні хімічні властивості кислот наведено в таблиці 3. Таблиця 3. Хімічні властивості кислот
|
Хімічні властивості |
Рівняння реакцій |
|
Змінюють забарвлення індикаторів (табл. 2) |
|
|
Взаємодіють з металами, розташованими в ряду активності лівіше від водню |
 |
|
Взаємодіють з основними оксидами з утворенням солі й води |
 |
|
Взаємодіють з основами з утворенням солі й води |
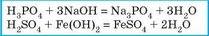 |
|
Взаємодіють із солями, якщо в результаті реакції виділяється газ, утворюється осад або вода |
 |
Основи
Основи — сполуки, що складаються з атомів металічного елемента та однієї або декількох гідроксильних груп OH.
Загальна формула основ:

За розчинністю у воді основи класифікують на дві групи:
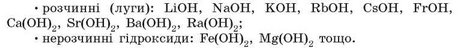
Основи зазвичай виявляють властивості, протилежні кислотам, тобто взаємодіють з речовинами з кислотними властивостями (табл. 4).
Таблиця 4. Хімічні властивості основ
|
Луги |
Нерозчинні гідроксиди |
|
Змінюють забарвлення індикаторів (табл. 2) |
Не змінюють забарвлення індикаторів |
|
Взаємодіють з кислотами з утворенням солі й води (реакція нейтралізації): 2KOH + H2SO4 = K2SO4 + 2H2O |
Взаємодіють з кислотами з утворенням солі й води: Fe(OH)2 + H2SO4 = FeSO4 + 2H2O |
|
Луги |
Нерозчинні гідроксиди |
|
Взаємодіють з кислотними оксидами: |
Взаємодіють з кислотними оксидами, які відповідають сильним кислотам: |
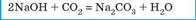 |
 |
|
Взаємодіють з амфотерними оксидами й гідроксидами: |
Взаємодіють з амфотерними оксидами й гідроксидами під час сплавляння: |
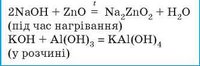 |
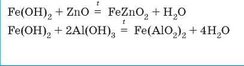 |
|
Взаємодіють з розчинами солей, якщо утворюється нерозчинна речовина (випадає осад): |
Із розчинами солей зазвичай не взаємодіють |
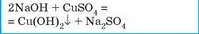 |
|
|
Гідроксиди лужних елементів під час нагрівання не розкладаються; гідроксиди лужноземельних розкладаються, але за значно більшої температури, ніж нерозчинні гідроксиди: |
Під час нагрівання розкладаються з утворенням оксиду та води: |
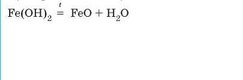 |
|
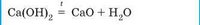 |
Солі
Солі можна розглядати як продукти заміщення в кислоті атомів Гідрогену на атоми металічних елементів або заміщення в основах гідроксид-іонів на кислотний залишок.
Солі — сполуки, що складаються з атомів металічних елементів і кислотних залишків.
Загальна формула солей:

Солі зазвичай вступають у реакції обміну з іншими речовинами (табл. 5, с. 10). Реакції обміну відбуваються за умови, якщо в результаті взаємодії утворюється осад, газ чи вода.
Таблиця 5. Хімічні властивості солей
|
Хімічні властивості |
Рівняння реакцій |
|
Взаємодіють з кислотами, якщо утворюється слабкіша чи нестійка кислота або осад |
 |
|
Розчинні солі взаємодіють з лугами, якщо утворюється осад |
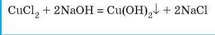 |
|
Розчинні солі вступають у реакції обміну одна з одною, якщо утворюється осад |
 |
|
Розкладаються під час нагрівання, якщо утворюються леткі оксиди |
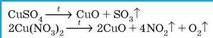 |
|
Активніші метали здатні витісняти менш активні метали з розчинів солей |
 |
Контрольні запитання
1. Дайте визначення оксидам, кислотам, основам і солям. За якими ознаками іх класифікують на групи? Наведіть приклади.
2. Які метали здатні витісняти водень з кислот?
3. Сформулюйте умови, за яких відбуваються реакції обміну у водних розчинах. Наведіть приклади реакцій.
4. Які сполуки належать до амфотерних? Наведіть приклади.
Завдання для засвоєння матеріалу
5. Складіть формули таких оксидів: калій оксид, фосфор(ііі) оксид, аргентум(І) оксид, ферум(іі) оксид, хлор(іУ) оксид, нітроген(У) оксид, цинк оксид, аурум(ііі) оксид.
6. Доповніть схеми реакцій, доберіть коефіцієнти, запишіть назви продуктів реакцій:
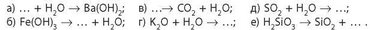
7. Складіть рівняння реакцій між кислотою та гідроксидом, у результаті яких утворюються такі солі: K2SO4, Mg(NO3)2, ZnSO4, CaCl2, Al(NO3)3.
8. Складіть рівняння реакцій, що відповідають таким перетворенням:
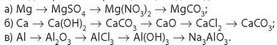
9. Порівняйте об'єми сульфур(іУ) оксиду (н. у.), який можна добути із сірки масою 480 г та натрій сульфіту масою 630 г.
10. Обчисліть масу фосфору, яку необхідно ввести в низку перетворень для добування кальцій ортофосфату масою 15,5 г.
11. Для побілки стовбурів плодових дерев використовують вапняне молоко: суміш 2 кг гашеного вапна Са(ОН)2 та 10 л води. Обчисліть масу кальцій оксиду, необхідного для добування гашеного вапна такої кількості.
12. Для чищення каналізаційних труб використовують рідкий засіб, що містить 40 % натрій гідроксиду, у кількості 250 г розчину на кожне місце очищення. Одне упакування з таким сухим засобом містить 70 г натрій гідроксиду. Визначте, скільки таких упакувань вам необхідно придбати, щоб прочистити труби: раковину на кухні, рукомийник у ванній, злив душової кабінки.