Вспомните: какие реакции называют качественными и для чего их используют (§ 13).
Формула глицерола
В природе встречаются спирты, молекулы которых содержат больше одной гидроксильной группы -OH. В названиях таких спиртов наличие групп -OH также обозначают суффиксом -ол-, но чаще для них используют традиционные названия. Самый распространенный в природе такой спирт — глицерол (или глицерин). Это самый простой трехатомный спирт, молекулы которого содержат три гидроксильных группы. Согласно химической номенклатуре, он называется пропантриол:

Обратите внимание, что в молекуле глицерола гидроксильные группы связаны с разными атомами Карбона. Две гидроксильные группы не могут быть присоединены к одному атому Карбона — такие вещества нестабильны и при образовании сразу же разлагаются.
Вместе с метанолом и этанолом глицерол является одним из первых спиртов, которые активно изучались химиками. Они проявляют достаточно высокую химическую активность, благодаря чему было открыто много закономерностей, над которыми работали А. П. Эль-теков, А. М. Зайцев, В. В. Марковников и другие.

Выдающийся украинский химик-органик. В 1868 году окончил Харьковский университет, в котором работал до конца жизни. Основные труды посвящены определению строения и изучению превращений углеводородов и их оксигенсодержащих производных (спиртов и эфиров). Пришел к выводу о неустойчивости некоторых ненасыщенных спиртов, и, основываясь на этом, сформулировал правило, которое сегодня называют его именем — правило Эльтекова (через несколько лет к тому же выводу пришел Эрленмейер, поэтому это правило также называют правилом Эльтекова-Эрленмейера). Разработал метод синтеза высших углеводородов, который сегодня является основой синтеза некоторых видов моторного горючего.
Молекулярная формула глицерола — C3H8O3, но ее обычно не используют, поскольку она не отражает химической сути вещества. Иногда молекулярную формулу глицерола записывают так: C3H5(OH)3.
Физические свойства глицерола
Глицерол — бесцветная сиропообразная, очень вязкая жидкость (среди всех известных жидкостей у глицерола вязкость наибольшая), не ядовит. Температура плавления — 17,8 °С, температура кипения — 290 °С. Глицерол нелетуч, тяжелее воды (плотность — 1,26 г/мл), неограниченно растворим в воде (смешивается в любых соотношениях). Гли-церол очень гигроскопичен (поглощает водяной пар из воздуха), сладкий на вкус, за что и получил свое название (от греч. glykos — сладкий).
Подобно одноатомным спиртам, молекулы глицерола также образуют водородные связи, но каждая молекула глицерола может образовать по девять таких связей, что отражается на его физических свойствах: чрезвычайная вязкость, неограниченная растворимость. Температура кипения глицерола так высока, что лежит на границе возможности существования органических соединений: при такой температуре органические вещества разлагаются, и глицерол не исключение, при сильном нагреве он начинает дымить и выделять ядовитые продукты разложения.
Химические свойства глицерола
Горение. Как и большинство органических веществ, глицерол горит в воздухе. Но благодаря значительному количеству водородных связей между молекулами глицерол нелетуч, и для горения жидкость

должна сначала испариться. Поэтому глицерол горит после нагревания:
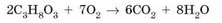
Качественная реакция на глицерол. Отличить глицерол, как и другие многоатомные спирты, от одноатомных можно при помощи качественной реакции. Качественной реакцией на глицерол является его взаимодействие со свежеосажденным (только полученным) купрум(П) гидроксидом.
Атомы Купрума замещают атомы Гидрогена в гидроксильных группах.
В результате реакции при добавлении к голубому осадку купрум(П) гидроксида раствора глицерола образуется прозрачный темно-синий раствор соединения Купрума с глицеролом (рис. 32.1).
Упрощенно формулу образованного соединения можно записать так:
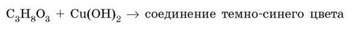
Аналогично купрум(П) гидроксид взаимодействует и с другими многоатомными спиртами.
При изучении свойств только что открытого глицерола Карл Шееле решил воздействовать на него концентрированной сульфатной кислотой. Во время реакции по комнате начал распространяться едкий запах, от которого у ученого случилось обильное слезотечение. Так был получен акролеин (в переводе с греческого — «острое масло»). Акролеин также обусловливает запах подгоревшего жира в затухающих сальных свечах.
Применение глицерола
Применение глицерола основано в первую очередь на его гигроскопичности. Благодаря ей он смягчает кожу, поэтому его используют в кожевенном производстве и для изготовления косметических средств. Глицерол добавляют в кондитерские изделия, чтобы те дольше не черствели, и к газированным напиткам в качестве подсластителя. Благодаря вязкости и низкой температуре плавления глицерол используют при изготовлении тормозных жидкостей и антифризов. Из глицерола получают тринитроглицерол, являющийся основой взрывчатки и медицинского препарата для лечения сердечных заболеваний.

Рис. 32.2. Применение глицерола
ЛАБОРАТОРНЫЙ ОПЫТ № 11
Взаимодействие глицерола с купрум(11) гидроксидом
Оборудование: штатив с пробирками, пробиркодержатель, горелка.
Реактивы: растворы глицерола, CuSO4, NaOH (или KOH).
Правила безопасности:
• для опытов используйте небольшие количества реактивов;
• при нагревании не прикасайтесь руками к горячим предметам;
• остерегайтесь попадания реактивов на кожу, в глаза, на одежду; при попадании едкого вещества смойте его большим количеством воды и протрите поврежденное место разбавленным раствором боратной кислоты.
1. Получите купрум(П) гидроксид: в пробирку налейте раствор щелочи объемом 1-2 мл и добавьте несколько капель раствора купрум(П) сульфата.
2. К образовавшемуся осадку добавляйте по капле раствор глицерола до растворения осадка купрум(П) гидроксида. Перемешайте смесь. Что происходит? В какой цвет окрашивается раствор?
3. Полученный раствор осторожно нагрейте в пламени горелки. Что происходит? Сформулируйте признак качественной реакции на глицерол.
Ключевая идея
Увеличение числа гидроксильных групп в молекуле наглядно иллюстрирует закон перехода количественных изменений в качественные: принципиально свойства не меняются, но те, что есть, проявляются по-другому.
Контрольные вопросы
378. По какому признаку соединения относят к многоатомным спиртам?
379. Охарактеризуйте физические свойства глицерола. Чем они отличаются от свойств одноатомных спиртов. Чем это обусловлено?
380. Приведите молекулярную формулу глицерола. Производным каких углеводородов он является?
381. В чем сходно и чем отличается горение глицерола от горения этанола? Составьте соответствующие уравнения реакций.
382. Опишите применение глицерола. На каких свойствах основано его применение в различных сферах?
Задания для усвоения материала
383. Докажите, что глицерол — это насыщенное соединение.
384. Сравните физические свойства этанола и глицерола. Объясните, как водородные связи влияют на схожесть и различие их свойств.
385. В двух пробирках содержатся две жидкости — этанол и глицерол. Как можно их различить? Составьте план проведения опыта.
386. Сравните объемы кислорода, необходимые для сжигания этанола и глицерола массой по 1 г. В каком случае кислорода израсходуется больше?
387. Для приготовления увлажняющего раствора рекомендуют смешать одну чайную ложку глицерола с тремя столовыми ложками воды. Определите массовую долю глицерола в таком растворе, если в чайную ложку помещается около 5 мл жидкости, в столовую — 15 мл. Другие необходимые данные найдите в тексте параграфа.
388. Косметические препараты для увлажнения кожи на основе глицерола рекомендуют применять при влажности воздуха более 65 %, поскольку при меньшей влажности такие препараты, наоборот, высушивают кожу. Объясните этот факт.
389*. В дополнительных источниках найдите информацию о составе и области применения антифризов. На каких свойствах глицерола основано его использование в таких смесях?
Это материал учебника Химия 9 класс Григорович